QUÍMICA SAN MARCOS SOLUCIONES DE ADMISIÓN
PREGUNTA 84 :
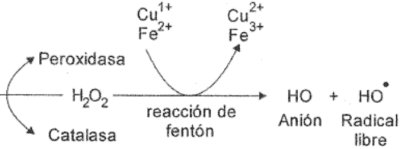
Los radicales libres son especies químicas muy agresivas; se los representa con un punto en su fórmula química. Muchos radicales libres oxigenados se forman a partir del peróxido de hidrógeno, molécula que nuestro cuerpo trata de destruir ni bien se forma, como se aprecia en el siguiente esquema:
Datos: 29Cu, 26Fe
Respecto de lo señalado, es correcto afirmar que el
A) ion férrico es agente oxidante
B) radical libre presenta igual configuración electrónica que el anión.
C) último electrón del Cu1+ tiene los números cuánticos (3, 2, +1, +1/2).
D) catión ferroso tiene más electrones desapareados que el catión férrico.
E) oxígeno del anión completa el octeto.
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 85 :
El pH de la sangres es 7,40 y permanece casi invariable, debido a diferentes mecanismos de autorregulación, que se rigen por el principio de Le Chatellier. Un ejemplo de ellos es el sistema bicarbonato (la presión de CO2 se regula a través de la ventilación pulmonar), el cual se puede considerar formado por varios equilibrios:
En una hiperventilación (ventilación pulmonar profunda) se elimina CO2, el equilibrio se desplaza hacia la y el pH porque la concentración de protones. Cuanto menor sea la eliminación de CO2 será la concentración de ácido carbónico.
A) izquierda - aumenta - disminuye - mayor
B) derecha - aumenta - aumenta - mayor
C) izquierda - disminuye - disminuye - menor
D) derecha - aumenta - disminuye - menor
E) izquierda - disminuye - aumenta - mayor
RESOLUCIÓN :
EQUILIBRIO QUÍMICO – PRINCIPIO DE LE CHATELIER
La hiperventilación es un tipo de respiración más profunda y más rápida de lo normal, que hace que la cantidad de dióxido de carbono (CO2) en la sangre baje demasiado. Esto podría provocar aturdimiento, latidos cardíacos rápidos, falta de aire, entumecimiento u hormigueo en las manos o los pies, ansiedad, desmayos y dolor en los músculos pectorales.
Algunas causas de la hiperventilación incluyen ansiedad extrema, asma, enfisema, lesión en la cabeza, fiebre, exposición a alturas de más de 6000 pies (2000 m) y algunos medicamentos.
El cuerpo en estos casos debe aumentar la cantidad de CO2, de forma mecánica (respirando el propio CO2 exhalado en la respiración) y así restablecer el equilibrio
De lo anterior, podemos decir que: “en la hiperventilación, se elimina el CO2 y el equilibrio de desplaza hacia la izquierda, y el pH aumenta, por que disminuye la concentración de protones, cuanto menor sea la eliminación de CO2 mayor será la concentración del ácido carbónico”.
Rpta. : "A"
PREGUNTA 86 :
Se le pide a una persona preparar 500 mL de una solución que contenga 142 mEq/L de ion sodio y 4,2 mEq/L de ion potasio a partir de una solución de NaCl 0,9 M y KCl 0,5 M. ¿Qué volumen de las soluciones, respectivamente, se deben diluir al volumen requerido?
A) 39,5 y 2,0
B) 157,8 y 8,4
C) 78,9 y 4,2
D) 90,0 y 4,2
E) 78,9 y 8,4
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 87 :
El hexano es el nombre del hidrocarburo saturado de seis átomos de carbono. Presenta varios isómeros. Compare las fórmulas de los siguientes isómeros del hexano y marque la afirmación correcta referida a sus propiedades física y químicas.
A) Son compuestos polares debido al enlace simple carbono- carbono.
B) En (a) hay cuatro carbonos primarios y dos carbonos secundarios.
C) La estructura (b) sufre reacciones de eliminación al igual que sustitución.
D) El isómero (c) es un buen combustible y sólido a temperatura ambiente.
E) Las fuerzas de London son de mayor intensidad en (a) que en los otros isómeros.
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 88 :
La naturaleza humana está constituida, principalmente, a base de cuatro elementos químicos: C, H, O y N. Estos elementos no metálicos se enlazan covalentemente y construyen diversas estructuras químicas.
Por ejemplo:
Al respecto, determine el valor de verdad (V o F) de las siguientes proposiciones:
I. Cada uno de los átomos de nitrógeno tiene un par de electrones libres.
II. El grupo hidróxido forma puente de hidrógeno con el agua y se ioniza.
III. Están presentes cuatro carbonos con hibridación sp2.
IV. Las tres estructuras son heterocíclicas y aromáticas.
A) VFFV
B) VVFF
C) FVVV
D) VFFF
E) FVVF
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 89 :
Se somete a electrólisis el agua, acidulada con ácido sulfúrico, para lo que se emplea una corriente de 965 amperios por 10 segundos. Determine el volumen, en litros, de la mezcla gaseosa formada a 25°C y 1 atm de presión.
Datos: H=1 g/mol, O=16 g/mol, R=0,082 atm – L mol K
A) 1,2
B) 2,4
C) 1,8
D) 3,6
E) 1,5
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 90 :
La oxidación de la glucosa a nivel intracelular e industrial en el nivel C1, genera ácido glucónico. Su reducción en el mismo carbono genera el sorbitol, sustancia de elevada viscosidad y de menor poder edulcorante. A continuación, se presenta algunas ecuaciones químicas referidas a las transformaciones mencionadas.
Al respecto, determine la alternativa correcta.
A) El sorbitol es un compuesto muy poco soluble en el agua.
B) El carbono 1 del ácido glucónico forma éteres con alcoholes y/o fenoles.
C) La dextrosa y el sorbitol forman estructuras cíclicas más estables.
D) El gluconato de isopropilo es insoluble en agua.
E) El carbono 1 de la glucosa y del ácido glucónico tienen igual hibridación.
RESOLUCIÓN :
Rpta. : "B"
SEGUNDA PRUEBA
PREGUNTA 105 :
El cloruro de magnesio (MgCl2)(12Mg, 17Cl) es una sal haloidea que se usa como lubricante de hilos, como suplemento alimenticio, en la fabricación de papel, etc. Identifique sus configuraciones electrónicas de catión y anión, respectivamente.
A) 1s² 2s²2p⁶ ; 1s²2s²2p⁶3s²3p⁶
B) 1s²2s²2p⁶3s¹ ; 1s²2s²2p⁶3s²3p⁵
C) 1s²2s²2p⁶3s¹ ; 1s²2s²2p⁶3s²3p⁶
D) 1s²2s²2p⁶1s² ; 2s²2p⁶3s²3p⁵
RESOLUCIÓN :
Rpta. : "A"
PREGUNTA 106 :
Cerca del 70% en masa de nuestro cuerpo es agua. Las moles y moléculas de agua, respectivamente, contenidas en el cuerpo de una persona que pesa 70 kg, son
Datos:
Elemento H O
uma 1 16
A) 3,88 ×10−³ y 2,34×10²¹
B) 2,72 ×10⁰ y 1,64×10²⁷
C) 2,72 ×10−³ y 1,64×10²¹
D) 2,72 ×10³ y 1,64×10²⁷
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 107 :
De una muestra de Na2CO3 impura, se pesan exactamente 5g de reactivo. Si se la hace reaccionar con una solución acuosa de cloruro de calcio y, luego de filtrarla y secar el precipitado, se obtiene 4,25 g de CaCO3 puro, determine el porcentaje de pureza de la muestra de Na2CO3 si la reacción que ocurre es
A) 94,3
B) 85,0
C) 80,0
D) 90,1
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 108 :
La unidad de polimerización, a partir de la cual se construye la fibra sintética orlon, se conoce como acrilonitrilo. Si la fórmula de esta molécula es
Determine el valor de verdad (V o F) de las siguientes afirmaciones:
I. Los carbonos 1 y 2 tienen hibridación sp2
II. El nitrógeno cumple con la regla del octeto.
III. El carbono número 3 tiene hibridación sp3
A) VVF
B) FVF
C) FFF
D) VFV
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 109 :
Se sabe que pequeñas cantidades de sales disueltas en el agua potable la hacen conductora de la corriente eléctrica. En la figura se representa una celda electrolítica que contiene agua potable, por la que se hace pasar la corriente eléctrica y se produce la electrólisis del agua según la ecuación
Establezca el valor de verdad (V o F) para los siguientes enunciados:
I. En el cátodo (–) ocurre la reducción y en el ánodo ( +) la oxidación.
II. Durante la electrólisis, se libera oxígeno gaseoso en el ánodo ( +).
III. En ambos electrodos se libera igual número de moles de H₂(g) y O₂((g).
A) VVV
B) FVF
C) VVF
D) VFV
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 110 :
Una de las mayores reservas de gas natural (GN) de América Latina se encuentra ubicada en los yacimientos de San Martín y Cashiriari, y es conocida como Lote 88-Camisea. Identifique la alternativa correcta referida al GN.
A) Es un recurso natural no renovable, formado casi en su totalidad por propano.
B) Su refinación constituye la etapa previa a su distribución al consumidor final.
C) Durante su combustión, emite a la atmósfera menores concentraciones de CO2
D) A diferencia de otro recurso natural no renovable, su combustión es incompleta.
RESOLUCIÓN :
RECURSOS NATURALES
El GN es una mezcla de hidrocarburos que presenta como principales componentes al metano CH4 (94 %), etano C2H6(3,9 %), propano C3H8(0,8 %) entre otros.
Constituye una importante fuente de energía fósil liberada por su combustión.
Es un combustible muy versátil y con menos emisiones de CO2, en comparación a otros combustibles.
Así, también su obtención o extracción es más sencilla y económica.
Rpta. : "C"