QUÍMICA UNI EXAMEN ADMISIÓN UNIVERSIDAD DE INGENIERÍA PROBLEMAS RESUELTOS PDF
PREGUNTA 21 :
Respecto a la teoría mecano-cuántica y la estructura atómica, ¿cuáles de las siguientes proposiciones son correctas?
I. El electrón ya no están en una órbita, en el sentido de Bohr, sino más bien hay una nube de probabilidad electrónica.
II. Cada uno de los estados cuánticos, diferenciados por n, l, ml, corresponde a distintas funciones de distribución de probabilidad (orbitales).
III. La función de probabilidad más sencilla se obtiene para los estado s (l=10) y tienen simetría esférica.
A) solo I
B) solo III
C) I y II
D) II y III
E) I, II y III
RESOLUCIÓN :
Tema: Modelo atómico del átomo
I. El electrón ya no está en una órbita, en el sentido de Bohr, sino más bien hay una nube de probabilidad electrónica.
Afirmación correcta.
II. Cada uno de los estados cuánticos diferenciados por n, l, ml, corresponde a distintas funciones de distribución de probabilidad (orbitales).
Afirmación correcta.
III. La función de probabilidad más sencilla se obtiene para los estados s (l =0) y tienen simetría esférica.
Afirmación correcta.
Rpta. : "E"
PREGUNTA 22 :
La fuerza electromotriz de una celda galvánica es independiente de
A) naturaleza de los electrodos.
B) concentración de los cationes.
C) concentración de los aniones.
D) temperatura del sistema.
E) volumen de los electrolitos.
RESOLUCIÓN :
Tema: Celda galvánica
La diferencia de potencial que se establece entre los dos electrodos de una celda galvánica también recibe el nombre de fuerza electromotriz (fem) de la celda galvánica.
ELECTROQUÍMICA
La diferencia de potencial entre los dos electrodos de una pila galvánica o voltaica, recibe el nombre de fuerza electromotriz o potencial estándar de pila, haciendo referencia a la denominación estándar, es decir, [ ]=1 m y T=298 K (25 °C).
La fem puede verse influenciada por factores como: naturaleza del electrodo, concentración de iones, temperatura entre otros.
Sin embargo, el volumen de los electrolitos no tiene influencia en el cálculo de la fem.
Rpta. : "E"
PREGUNTA 23 :
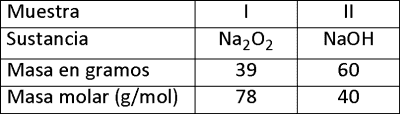
Dada la siguiente información:
Señale la alternativa correcta.
A) La muestra I corresponde a 1,5 mol de Na2O2.
B) La muestra II corresponde a 0,5 mol de NaOH.
C) Ambas muestras presentan igual número de moles.
D) La muestra I presenta mayor número de moles que la muestra II.
E) La muestra II presenta mayor número de moles que la muestra I.
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 24 :
En el horno eléctrico de una siderúrgica se coloca chatarra de acero y después de unos minutos se observa la formación de gases pardo-rojizos los cuales, en corto tiempo, se difunden en el área de trabajo y la zona aledaña. Por otro lado, el acero fundido obtenido en el horno, se vierte en moldes de madera. Pasado un tiempo, a partir del acero fundido se obtienen bolas de acero utilizadas en los molinos. ¿Cuántas de las observaciones subrayadas involucran cambios físicos y químicos, respectivamente?
A) 0, 4
B) 1, 3
C) 2, 2
D) 3, 1
E) 4, 0
RESOLUCIÓN :
Tema: Materia
Se pide reconocer si los cambios son a nivel físico o químico, lo que ocurre en el horno eléctrico de una siderurgia, donde se procesa una chatarra de acero (hierro oxidado).
Recordemos que la materia se encuentra en permanente cambio. Si el cambio es a nivel físico (la materia mantiene su composición), así como si el cambio es a nivel químico (la materia cambia su composición química). Entonces analizamos las observaciones subrayadas:
• Formación de gases pardo-rojizo: cambio químico
• Se difunden en el área de trabajo: cambio físico
• El acero fundido obtenido en el horno: cambio físico
• A partir del acero fundido se obtienen bolas de acero utilizadas en los molinos: cambio físico
Entonces hay tres cambios físicos y un cambio químico.
MATERIA
I. La formación de gases pardo-rojizos implica la aparición del NO2 que se forma a partir del N2 atmosférico por la alta temperatura en el horno (cambio químico).
II. La difusión del NO2 implica un cambio físico.
III. El acero fundido implica un cambio físico de sólido a líquido.
IV. Del acero fundido se obtiene bolas de acero, implica otro cambio físico de líquido a sólido.
Rpta. : "D"
PREGUNTA 25 :
¿Cuántos gramos de sulfato de cobre pentahidrato, CuSO4 · 5H2O, serán necesarios para preparar 250 mL de una solución 0,1 M de CuSO4?
Masa atómica: Cu=63,5; S=32; O=16; H=1
A) 3,99
B) 5,12
C) 6,24
D) 8,75
E) 10,23
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 26 :
Dados los siguientes procesos:
Indique la proposición correcta:
A) La primera energía de ionización del cloro corresponde a un proceso exotérmico.
B) La segunda energía de ionización del cloro es menor que la primera.
C) Es más fácil que el cloro pierda electrones que los gane.
D) La primera afinidad electrónica del cloro corresponde a un fenómeno endotérmico.
E) El ion Cl (g)− es más estable que el átomo de Cl(g).
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 27 :
Respecto al 3-metil-1-butino, ¿cuáles de las siguientes proposiciones son correctas?
I. Tiene 11 enlaces sigma (σ).
II. Presenta 3 enlaces pi (𝛑).
III. No presenta isomería geométrica.
A) I y II
B) II y III
C) solo I
D) solo II
E) solo III
RESOLUCIÓN :
Analizamos cada proposición.
I. Incorrecta
La molécula presenta 12 enlaces sigma
II. Incorrecta
La molécula presenta 2 enlaces pi
III. Correcta
Isomería geométrica no es característica de los alquinos, sino de los alquenos y cicloalcanos.
Rpta. : "E"
PREGUNTA 28 :
A 25 ºC, el agua de lluvia puede llegar a tener un pOH de hasta 12. En este caso, ¿cuántas veces mayor es la concentración de iones hidronio de esta agua con respecto al agua neutra?
A) 12/7
B) 2/7
C) 5
D) 10^5
E) 10^12
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 29 :
Una solución preparada mezclando 5 g de tolueno, C7H8, con 225 g de benceno, C6H6, tiene una densidad de 0,976 g/mL. Calcule la molaridad del tolueno en dicha solución.
Masas molares (g/mol): tolueno=92; benceno=78
A) 0,05
B) 0,11
C) 0,15
D) 0,23
E) 0,26
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 30 :
Dada la siguiente información de potenciales estándar de reducción, en voltios:
Indique la representación abreviada de la celda galvánica que puede construirse y que genere el mayor potencial (en voltios).
A) Ag(s) / Ag+(1 M) || Cu2+(1 M) / Cu(s)
B) Ag(s) / Ag+(1 M) || Ni2+(1 M) / Ni(s)
C) Cu(s) / Cu2+(1 M) || Ag+(1 M) / Ag(s)
D) Cu(s) / Cu2+(1 M) || Ni2+(1 M) / Ni(s)
E) Ni(s) / Ni2+(1 M) || Ag+(1 M) / Ag(s)
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 31 :
Los polímeros son grandes moléculas constituidas por una unidad fundamental (monómero) que se repite. Respecto a los tipos de polímeros, y siendo A y B dos monómeros, indique la relación correcta .
I. Homopolímero
II. Copolímero
III. En bloque
a. ~A – B – A – B – A – B ~
b. ~A – A – A – A – A – A ~
c. ~A – A – A – B – B – B ~
A) Ia, IIb, IIIc
B) Ic, IIb, IIIa
C) Ia, IIc, IIIb
D) Ib, IIc, IIIa
E) Ib, IIa, IIIc
RESOLUCIÓN :
POLÍMEROS
Los polímeros son macromoléculas formadas por unión mediante enlaces covalentes de uno o más tipos de unidades simples llamadas monómeros. Pueden clasificarse según su cadena como
Rpta. : "E"
PREGUNTA 32 :
¿Cuál de los siguientes compuestos representa a un aldehído?
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 33 :
Dada la siguiente reacción en medio acuoso
Señale la alternativa que corresponda a un par conjugado ácido-base según Bronsted-Lowry.
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 34 :
Una sustancia diamagnética, sin electrones desapareados, es ligeramente repelida por un campo magnético, mientras que una sustancia paramagnética, con electrones desapareados es atraída débilmente por un campo magnético. ¿Cuántas de las siguientes sustancias son paramagnéticas?
A) 1
B) 2
C) 3
D) 4
E) 5
RESOLUCIÓN :
Rpta. : "A"
PREGUNTA 35 :
Durante el fenómeno de la disolución pueden desarrollarse una serie de interacciones intermoleculares. ¿Cuáles de las siguientes son posibles?
I. Puente de hidrógeno
II. Ion-dipolo
lll. Dipolo-dipolo inducido
A) solo I
B) solo II
C) solo III
D) I y II
E) I, II y III
RESOLUCIÓN :
FUERZA INTERMOLECULARES
Durante el fenómeno de disolución se producen interacciones entre las moléculas y/o iones del soluto y las moléculas del solvente.
► Puente hidrógeno
► Ion - dipolo permanente
► Ion - dipolo inducido
► Dipolo permanente - dipolo permanente
► Dipolo permanente - dipolo inducido
► Dipolo instantáneo - dipolo inducido
Rpta. : "E"
PREGUNTA 37 :
El fósforo blanco (P4) es obtenido de acuerdo con las siguientes reacciones:
A) 1,1
B) 2,2
C) 2,6
D) 3,1
E) 3,3
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 39 :
Dadas las siguientes proposiciones referidas a las siguientes reacciones que ocurren a igual temperatura:
A) solo I
B) solo II
C) solo III
D) I y II
E) I, II y III
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 40 :
A continuación se presenta un diagrama de fases genérico. ¿En qué puntos, de los señalados, se observarán 2 fases?
A) I, III y V
B) II y IV
C) III y V
D) I y IV
E) I y III
RESOLUCIÓN :
Un diagrama de fase, es una representación gráfica de las condiciones de temperatura y presión a las que existen los sólidos, líquidos y gases, como fases únicas de los estados de la materia o como dos o más fases en equilibrio.
Las diferentes regiones del diagrama corresponde a una sola fase o estado de la materia. Las líneas curvas o rectas donde se juntan las regiones de una sola fase, representan dos fases en equilibrio. En dicho diagrama existe un punto, denominado el punto triple, en donde coexisten el estado sólido, líquido y gaseoso. Asimismo, podemos mencionar que la curva que separa las fases vapor-líquido termina en un punto denominado punto crítico.
Rpta. : "A"